Обсуждение участницы:Людмила Зимонина
Содержание |
Добро пожаловать!
Здравствуйте, Людмила Зимонина!
От имени участников проекта Letopisi.Ru приветствую Вас! Надеемся, Вы получите большое удовольствие, работая над созданием гипертекста.
Начните с оформления Вашей личной страницы, (образец оформления здесь! )
|
Ссылки, полезные для начинающих
Вы можете подписываться на страницах обсуждения, используя четыре идущие подряд знака тильды ~~~~ или нажав на соответствующую кнопку
--Владимир Слесарев 13:36, 20 октября 2010 (UTC) Для данной статьи нужно создать отдельную страницу. Название может быть таким: Атом - сложная частица, урок по химии из опыта работы Людмилы Зимониной (именно так - без кавычек!). -- Владимир Слесарев 13:36, 20 октября 2010 (UTC)Ответить можно здесь
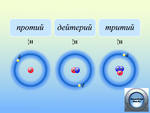
Урок химии "Атом - сложная частица"Цели урока:На основе межпредметных связей с физикой повторить доказательства сложного строения атома, модели, отражающие такое строение, строение атомного ядра и характеристику элементарных частиц (протонов, нейтронов и электронов). Рассмотреть на новом, боле высоком теоретическом уровне понятия «изотопы» и три формы существования химического элемента. Показать дуализм электронов, равно как и других объектов микромира. Рассмотреть квантовые характеристики электронов на основе четырех квантовых чисел и основные закономерности заполнения электронами атомных орбиталей. Развитие представлений о строении атома.Само понятие «атом» пришло к нам из Древней Греции и в переводе с греческого обозначает «неделимый». Обладая определенным багажом знаний из курсов физики и химии, каждый из вас может с уверенностью сказать, что слово «неделимый» не может быть применено к атому, поскольку со временем появились доказательства сложности строения атома. Вспомнить, какие? (открытие рентгеновских и катодных лучей, явление радиоактивности, фотоэффекта, электролиза и др.) Как шло развитие представлений о сложности строения атома, можно проследить по схеме на с. 4 (Схема 1). Знакомство с моделями Дж.Томсона «Пудинг с изюмом» планетарной Э.Резерфорда (Рис. 1 с. 3), квантовой (квант – порция энергии) Н.Бора (постулат – исходное положение). Модели Томсона, Резерфорда и Бора в настоящее время представляют лишь исторический интерес, так как внутренняя противоречивость и ограниченность этих моделей заставили вскоре отказаться от них. Нельзя автоматически переносить законы классической физики (например, таких ее разделов, как электродинамика и механика), справедливые для сравнительно больших тел, составляющих макромир, на ничтожно малые объекты – атомы, ионы, молекулы, электроны, протоны, нейтроны, фотоны, - образующие свой особый микромир. Задача описания свойств и поведения объектов микромира была решена только в ХХ веке после создания квантовой механики. Итак, современные представления о строении атома основываются на положениях квантовой механики, в 1932 году была разработана так называемая протонно-нейтронная теория ядра. 2. Строение атомного ядра.Что же представляет собой атом с точки зрения современных представлений? Прочитать определение с 5,, рассмотреть Рис. 2 с. 5. - Какие частицы входят в состав ядра? - Какое общее название они имеют? - Как определить число протонов и нейтронов в ядре на основании положения химического элемента в ПС Д.И.Менделеева? ПВ – Что следует ожидать, если в атомном ядре изменить число протонов - А нейтронов? Разновидности атомов одного и того же химического элемента, имеющие одинаковый заряд ядра, но разное массовое число, называются изотопами. (Записать). |